
분만사에서 신생 자돈 설사(Neonatal diarrhea, ND)는 현대 양돈 산업에서 가장 다루기 까다로운 문제다. 사양 관리 수준이 전반적으로 향상된 지금도 많은 농장주와 현장 관리자들은 분만사에서 가장 어려운 과제로 ‘초반 설사’를 지목한다.
설사는 임상적으로 눈에 잘 띄는 문제일 뿐 아니라, 한번 발생하면 초기 성장 정체를 일으키고 농장 수익성에도 적지 않은 부담을 남긴다. 더 중요한 점은, 신생 자돈 설사가 단순한 일시적 증상에 그치지 않는다는 사실이다.
생후 초기 자돈은 장 점막 면역이 아직 충분히 성숙하지 않았기 때문에, 작은 관리 실패나 병원체 노출도 더 큰 손실로 이어질 수 있다. 나아가 설사가 지속되면서 성장 여력이 떨어진 자돈은 이유 후 자돈사 구간에서 면역적으로 더 취약한 상태에 놓이게 되며, 이후 질병 위험 역시 커질 수밖에 없다.
실제 현장에서는 이 문제가 단순히 숫자로만 받아들여지지 않는다. 갓 태어난 어린 자돈이 설사로 활력을 잃고 점차 처지는 모습을 지켜보는 일은 관리자에게도 결코 가볍지 않으며, 그래서 신생 자돈 설사는 생산성의 문제이면서 동시에 관리자들의 마음을 무겁게 하는 문제이기도 하다.

포유자돈의 설사 문제를 이해할 때는 먼저 병원성 요인과 비병원성 요인을 함께 나눠 보는 접근이 필요하다. 비병원성 요인에는 환경 및 관리 조건을 살펴봐야 하는데, 대표적으로 초유 섭취 부족, 저체온, 분만사 위생 불량, 포유 불균형, 관리 스트레스가 포함된다.
반면 병원성 요인 가운데서는 장독소 생성 대장균(ETEC, Enterotoxigenic Escherichia coli)과 클로스트리디움 퍼프린젠스 A형(Clostridium perfringens type A, CpA)이 가장 실질적인 핵심 병원체로 많이 언급된다. 현장에서는 다양한 원인 후보를 열어두되, 실제로 먼저 확인하고 먼저 대응해야 할 대상은 이 두 병원체인 경우가 다분하다.
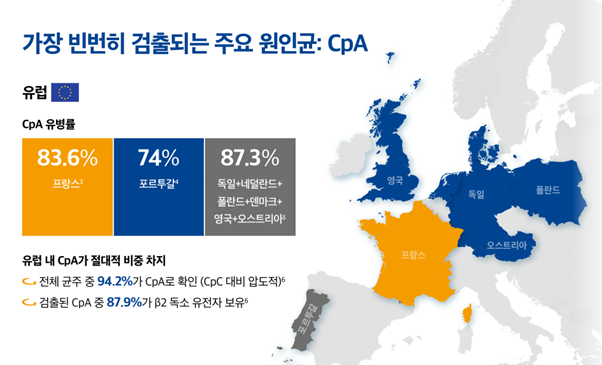

여러 가지 이유가 있겠지만 국내 자돈 설사에 관한 유병률의 자료의 흐름도 대체로 같은 방향을 보여준다. 포유자돈 설사 연구 사례에서 핵심 병원체를 분리해 보면, 반복적으로 중심에 놓이는 것은 대장균과 CpA다.
대장균은 생후 초기 수양성 설사와 탈수를 유발하는 대표 병원체로 잘 알려져 있고, CpA는 그에 비해 상대적으로 덜 알려졌지만 훨씬 더 해석이 까다로운 병원체다. 다만 분리 빈도와 현장 영향도를 함께 보면, 신생 자돈 설사를 논할 때 CpA를 뒤로 미루기는 어렵다. 결국 분만사 설사의 진단과 예방 전략의 변화는 대장균과 CpA를 중심으로 개편을 고민해 볼 필요가 있다.

특히 현장에서 중요하게 볼 부분은 α 독소와 β2 독소를 함께 고려하는 시각이다. 전통적으로는 α 독소를 중심으로 CpA의 병원성을 설명해 왔지만, 최근에는 포유자돈 설사에서 β2 독소 역시 실제 병원성에 관여하는 중요한 독소 인자로 더욱 분명하게 인식되고 있다.
β2 독소는 장 상피세포막에 기공을 형성해 세포막 기능을 무너뜨리고, 그 결과 상피세포 손상, 세포 사멸, 염증 반응, 장 점막 투과성 증가를 유도하는 것으로 보고된다. 이러한 변화는 장벽을 먼저 약화시키고 손상 범위를 넓혀, 결과적으로 α 독소에 의한 조직 손상과 혈관성 변화가 더 쉽게 확대될 수 있는 환경을 만든다.
따라서 CpA 관련 설사를 해석할 때는 단순히 “CpA가 검출되었다”는 사실에 그치기보다, α 독소와 β2 독소가 상호작용하며 병원성을 증폭시키는 구조로 이해하는 접근이 현장 판단에 더 도움이 된다. 포유자돈 설사라는 맥락에서 보면, α 독소와 β2 독소는 서로 따로 움직이는 독소라기보다, 장벽 손상과 병변 형성을 함께 키워가는 일종의 ‘팀플레이어’에 가깝다고 볼 수 있다.
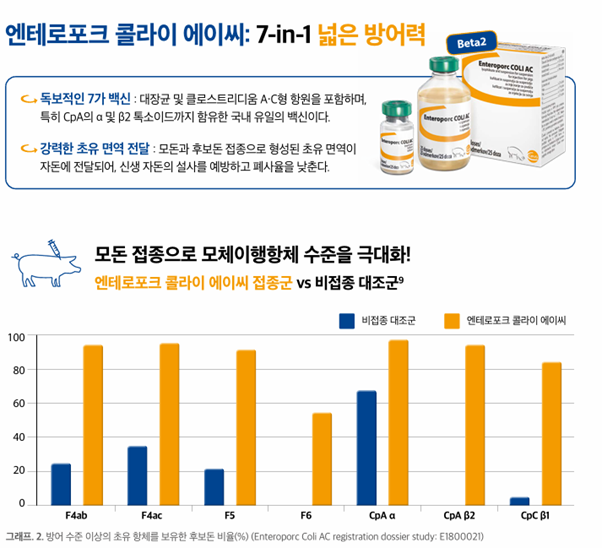
포유자돈 설사의 주요 원인이 독소 작용과 연결된다면, 예방 전략의 방향도 비교적 분명해진다. 신생 자돈은 스스로 충분한 면역을 형성할 시간이 부족하기 때문에, 실제 방어의 출발점은 자돈이 아니라 모돈이 된다. 생후 초기 자돈이 의존할 수 있는 가장 중요한 방어 수단은 초유를 통해 전달되는 수동 면역이기 때문이다. 따라서 분만사 설사를 줄이기 위한 면역 설계는 “설사한 자돈에 무엇을 할 것인가”보다, “모돈이 분만 전에 어떤 항체를 충분히 형성하고, 그것이 초유를 통해 자돈에게 효과적으로 전달될 수 있는가”에 더 달려 있다고 볼 수 있다.
그렇다면 현장에서 중요하게 봐야 할 질문은 하나다. 모돈의 강력한 초유 면역을 유도하기 위해, 백신 설계 시 어떤 항원을 포함해야 하는가 하는 점이다. 대장균에서는 주요 부착 인자와 독소가 중요하고, CpA에서는 독소 관련 항원이 방어 설계의 핵심이 된다. 특히 β2 독소 항원의 포함 여부는 매우 중요한 설계 포인트로 볼 수 있다. 최근 여러 연구에서 포유자돈 설사에서 CpA의 병원성을 논할 때 β2 독소는 반복적으로 핵심 위치를 차지해 왔고, 실제 방어 역시 단순히 “CpA를 포함하였다”는 수준이 아니라 어떤 독소까지 방어할 수 있느냐에 따라 달라질 수 있기 때문이다.
정리하자면, 신생 자돈 설사는 여러 요인이 복합적으로 얽혀 나타나는 문제이지만, 병원성 원인 측면에서는 대장균과 CpA를 먼저 보는 접근이 필요하다. 특히 CpA는 α 독소와 β2 독소를 함께 고려해야 실제 현장에 더 가깝게 해석할 수 있으며, 대응 전략 또한 자돈의 항생제 치료보다 모돈의 초유 면역을 어떻게 설계할 것인가에 더 큰 비중을 두어야 한다.
앞으로 본 시리즈에서는 이러한 관점에서 신생 자돈 설사에서의 CpA의 의미, 주요 독소의 생물학적 특징, 그리고 현장에서 적용할 수 있는 면역 설계의 핵심을 차례로 정리해 보고자 한다.
참고문헌
- Ceva Korea Survey, 2026
- Sjölund et al., 2014
- Jardin et al. 2021
- Nunes et al. 2021
- Ullerich et al.
- Springer et al., 2012
- Postbio Survey, 2023–2025
- Carvajal et al., 2019
- Enteroporc Coli AC dossier, E180021
세바코리아에서 유럽 ASF 차단방역 전략 영상과 가이드북(PDF)을 무료로 공유합니다.
세바코리아 카카오톡 채널을 통해 간편하게 요청해 주세요.
※ 위 기고 내용과 관련하여 궁금하신 사항은 세바코리아 (02-2203-9488 / 카카오톡채널: 세바코리아(바로가기) / ceva.korea@ceva.com)로 문의주시기 바랍니다.



