본 원고는 지난 5월 18/19일 한국양돈연구회 주최 '제19회 신기술양돈워크숍'에서 발표되었습니다.

1. 2017년 구제역 상황 리뷰
A. 2017년 첫번째 구제역 발생 (보은)
2017년 2월 5일, 충청북도 보은군 마로면 관기리에 위치한 195두 규모의 젖소 농장에서 구제역 의심신고가 접수되었다. 15마리는 침흘림을 보였고 5두는 유두에 수두가 관찰되었다. 증상으로만 보면 거의 확실한 구제역이었다. 정밀검사 결과는 당일 저녁 8시쯤 나올 예정이었지만 이미 전두수 살처분 준비가 시작되었다. 500미터 이내에 돼지 농장은 없었지만 소 농장이 12호 655두가 있었고 3km 이내에 소 농가 83호 (4,191두), 돼지 농가 4호 (5,141두)가 분포하고 있어 초동방역에 실패하면 주변 지역으로 퍼져나갈지도 모르는 상황이었다.
정부는 충북 보은의 첫번째 구제역 케이스가 구제역으로 확진되었음을 발표하면서 전국의 소 구제역 항체 양성율이 97.5%라는 브리핑 내용을 함께 발표했다. 하지만 나중에 실시된 구제역 ELISA 항체가 검사에서 O형에 대한 항체 양성율은 20% (4/20), A형에 대한 항체 양성율은 15%로 매우 낮게 나왔다. 도축장 출하 검사에서도 항체양성율 체크를 하고 있고 정부 기관에서는 전국 항체 양성율이 97.5%라고 파악하고 있었기 때문에 어떻게 이렇게 낮은 항체 양성율 농장이 존재할 수 있는지에 대해서 관심이 쏠렸다.
B. 보은에서 130km 떨어진 정읍에서 하루차이로 발생
전라북도 정읍은 충청북도 보은과 직선거리로 약 130km 이상 떨어진 곳이다. 그런데 정읍의 49두 사육규모의 한 한우 농가에서 두번째 구제역이 발생하였다. 두 농장간 거리가 워낙 멀고 역학적으로 연결할 수 있는 부분이 확실하지 않은데다가 거의 동시에 발생해서 우리가 알지 못하는 유인이 있을 가능성이 있다는 합리적인 의심을 갖게 한다.
2014년에서 2016년까지 국내에서 발생했던 구제역 바이러스는 O SEA Mya-98 유전형이었는데 이번에 발생한 보은 케이스와 정읍 케이스는 O ME-SA Ind 2001 유전형이었다. 이 말은 이번에 발생한 구제역 바이러스가 그동안 우리나라에 숨어 있던 바이러스가 아니라 새로 해외로부터 유입되었을 가능성이 높다는 것을 의미하는 것이기도 했다.
보은과 정읍 바이러스의 유전자를 분석해 보니 VP1 유전자 기준, 4개의 유전자 차이가 발견되었다. 4개의 유전자 차이가 1~3일만에 생길 수는 없는 것이어서 우리가 알지 못하는 원발 농장이 별도로 있거나 우리가 알지 못하는 오염원이 있을 수도 있다는 추측을 하게 했다.
정읍 케이스 역시 정읍에서 첫번째 케이스였기 때문에 전 두수 살처분을 진행하였는데 살처분하면서 채혈한 혈청에 대해 항체 양성율을 검사해보니 항체 양성은 20두 중 한 마리에 불과해서 5%의 양성율을 보였다. 소의 경우 돼지와 달리 백신을 접종하면 거의 100%에 가까운 항체 양성율이 나와야 정상인데 항체 양성율이 5%라는 것은 백신이 접종 되지 않았다는 것을 의미했다. 해당 농장주는 백신을 접종한 것으로 알고 있다고 언급하여 혹시 백신의 효능이 부족해서 생긴 일은 아닌지에 대한 언론보도가 있었으나 이는 곧 사실이 아닌 것으로 밝혀졌다. 백신접종 전 보은지역 항체 양성율이 30% 였는데 백신을 접종하고 양성율이 90%가 된 것이다. 문제는 어떻게 이렇게 낮은 항체 양성율을 가진 농장이 발견되지 않고 아무런 조치가 취해지지 않았는가 하는데 있다. 백신을 공급했다고 백신이 모두 접종되는 것은 아니다. 반드시 항체 검사를 통해 백신 항체 양성율을 체크해야 한다. 백신 보관이 잘못되거나 접종방법이 잘못되어 접종을 해도 백신효과가 나오지 않을 수도 있기 때문이다. 백신 항체 양성율 모니터링만 철저히 진행되었더라면 이번 구제역 사태는 충분히 막을 수 있었을지도 모른다.
C. 연천 A형 구제역의 발생으로 양돈업계가 패닉상태에 빠지다
2017년 2월 8일, 경기도 연천군 군남면 선곡리의 한 젖소농가에서 구제역 의심신고가 접수되었다. 젖소 114두를 키우는 농장이었는데 10두에서 침흘림 및 수포가 발견되었다. 처음에는 보은-정읍에 이은 3차 발생이라고 생각되었지만 280km나 멀리 떨어진 곳이라 매우 의외라고 생각하고 있었다. 그러나 살처분과 동시에 실시된 바이러스 실험에서 연천 구제역 바이러스는 지금까지 발생했던 O형 구제역이 아니라 A형 구제역이라는 사실이 밝혀졌다. 갑작스러운 A형 구제역의 등장에 놀란 것은 방역 당국 뿐만이 아니었다. 축산인들과 수의사들도 모두 패닉상태에 빠졌다. 왜냐하면 우리나라는 2016년 이후 소에만 O형과 A형 구제역 항원을 접종하고 있고 돼지에는 O형 항원만 접종하고 있었기 때문에 만약 연천 A형 구제역 항원이 돼지에 감염되기 시작한다면 2010년 구제역 대재앙이 다시 재현될 수도 있는 위급한 상황이었다.
엎친데 덮친 격으로 전국에 배포되어 있는 O형 + A형 백신의 재고를 급하게 파악해보니 전체 사용 가능한 물량이 불과 141만두 분 밖에 안되었다. 약 1,100만두 정도 되는 돼지와 약 300만두 되는 소 전체에 접종할 물량에는 크게 부족한 셈이었다. 2017년 2월말에 추가로 도입 가능한 물량 160만두를 포함해도 300만두 정도여서 선별적인 사용이 필수적이었다. 이미 2010년 구제역을 생생하게 겪었던 언론에서는 집중적으로 백신 부족 문제를 성토하기 시작했다.
2015년 8월, 정부는 구제역 백신 항원을 결정하기 위한 전문가 회의를 개최했다. 이 회의에 배석한 많은 전문가들은 소와 돼지에 O+A형 항원 사용을 주장했다. 하지만 백신의 직접적인 사용자인 한돈협회는 지금 당장 문제가 되는 O 형 문제가 시급하기 때문에 돼지는 항원이 강화된 O형 백신의 사용을 강력히 주장했고 생산자 단체의 주장은 받아들여 졌다. 하지만 앞으로의 리스크를 줄이기 위해 대신 차선책으로 소에는 O+A형 항원을 접종하기로 했다.
이 결정에는 여러 가지 과학적인 배경이 깔려 있었다. 우리나라를 둘러싼 주변국에서의 구제역 발생 통계를 보면 약 70% 정도가 O형 구제역이며 20% 정도가 A형, 10% 정도가 SAT1 형인데 이 SAT1형은 주로 중동지역에서 발생하고 있다. 그런데 그 A형 구제역도 발생국가의 통계를 보면 거의 대부분 소에서 발생하고 있었다. 물론 중국에서는 A형 구제역이 돼지에서도 발병한 케이스가 있었지만 소에서의 발생이 압도적으로 많았다. 전문가들이 선택한 차선이란, 야외에 노출되어 있고 돼지보다 1/25 만큼 적은 양이 바이러스 만으로도 감염이 가능한 소에 백신을 접종함으로써 돼지로의 전파를 막을 수 있는 방법을 선택한 것이었다. 2016년 이후로 그렇게 돼지에서는 A형 항원이 빠진 백신이 공급되었다. 그래서 만약 돼지로 A형 구제역이 발병하게 된다면 마른 장작에 불이 옮겨 붙은 것처럼 번지게 될 수 있는 상황이라 초긴장상태가 되었다.
■ 표 1. 2016년 10월부터 12월까지 WRLFMD에 보고된 구제역 요약표. 총 107개의 샘플이 접수되었는데 이중에서 37개의 바이러스가 분리되었는데 27개는 O형, 7개는 A형, 나머지 3개는 SAT1형이었다. 이 SAT1형은 나이지리아, 즉 아프리카 대륙에서 분리되었다.

추가적인 역학조사과정에서 연천 젖소 농가의 농장주가 2016년 9월 베트남 관광을 다녀왔다는 소식도 언론에 공개되었다. 그러나 해당 축산 농가에서 구제역 발생 직전에 해외여행을 간 것도 아니고 2개월 ~ 5개월 전에 동남아시아 해외 여행 간 것은 구제역과 연관시키지 않는 것이 합리적이라고 생각한다. 동남아시아를 가서 축산현장을 방문한 것도 아니고 일반 관광지를 방문하고 온 것인데 어떻게 구제역의 원인이 될 수 있겠나? 만약 원인이 될 수 있다 하더라도 여행다녀와서 바로 문제가 되어야지 어떻게 2~5개월 동안 문제가 없을 수 있겠나 하는 것이다. 축산 선진국에서는 구제역 발생국가인 한국에서 왔다고 해도 농장 방문전 충분한 기간이 있었으면 농장 방문도 허락해 준다. 동남아시아 여행이 구제역의 원인이라면 한 해에 1000만명 넘는 관광객이 방문하고 중국 등 구제역 발생 국가에서 약 250만명이 방문하는 제주도는 왜 구제역 발생이 없는지 생각해 보아야 한다.
그 밖에도 연천 A형 구제역 발생 건은 또 다른 특징을 가지고 있는데 살처분시 채혈한 20개의 혈청을 분석한 결과 O형 항체 양성율은 52%였는데 A형 항체 양성율은 90%였다. 통계적으로 보면 O형 항원의 양성율과 A형 항원의 양성율이 서로 비슷한 수준인 경우가 대부분이어서 이미 항체가가 생긴 다음에 신고가 된 것은 아닌지 의혹을 받았으나 신고가 접수된 2017년 2월 8일 이후 6일이 지났지만 아직 연천 주변으로 A형 구제역 발생신고는 없는 상태이다.
D. 충청북도 보은 지역에 집중된 구제역 발생
이번 구제역의 경우 보은지역에만 총 7건의 발생이 보고되고 있다. 모두 최초 발생 농장으로부터 반경 3km 이내에 있고 모두 소를 키우는 농장이다. 2017년 2월 12일에 보고된 자료에 따르면 이 지역의 소 항체 양성율은 71%였다. 2월 7일까지 완료된 백신 항체가 유도될 때까지는 추가 발생이 염려되는 이유이다. 일반적으로 구제역 백신을 접종하면 1주일 뒤면 항체가가 유도되기 시작한다. 물론 2주가 지나야 충분한 항체가가 형성된다. 여기서 한가지 더 추가로 짚고 넘어갈 부분은 바로 백신의 효능 부분이다. 최근 항체가 100%였음에도 불구하고 구제역에 걸린 사례가 있다며 또 ‘물백신’ 논란이 일고 있다. 필자의 소견으로는, 현재 사용하고 있는 백신은 사독백신이기 때문에 100% 완벽한 방어는 할 수 없지만 그래도 충분히 백신으로서의 효능을 가지고 있다고 평가한다. 만약 지금 쓰고 있는 백신들이 효능이 없었다면 지금의 상황은 훨씬 더 좋지 않았을 것이다. 구제역 발생 농장에서 부분적 살처분을 해도 나머지 개체들이 추가로 발생하지 않는 것은 백신이 방어를 해주었기 때문이다. 그리고 지금까지는 백신의 효능이 크게 부족해서 문제가 되고 있다는 증거를 찾지 못했다.
2. 최근 양돈 질병 동향
A. 2016년 대한민국 질병 진단 결과 요약
본 자료는 ㈜옵티팜에 의뢰된 케이스 중 2016년 1월 1일부터 2016년 12월 31일까지의 데이터를 전년도 동기간과 비교하였다. 통계는 ㈜옵티팜 홈페이지가 자동으로 생성하는 통계 기능 기반으로 분석되었다.
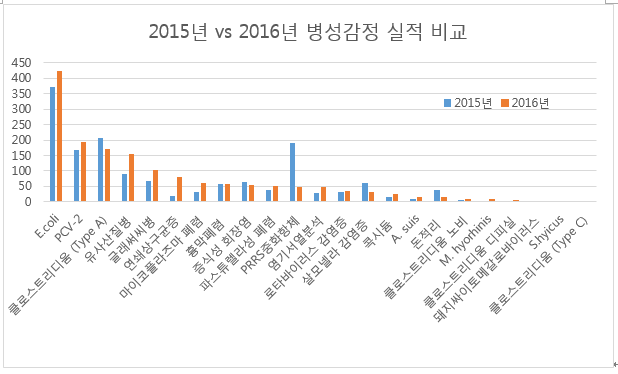
그림 1. 필자가 몸담고 있는 ㈜ 옵티팜에서 지난 1년간 진단된 케이스를 정리하여 위와 같이 그래프로 표시하였다. 가장 빈번하게 농장에서 볼 수 있는 케이스부터 순서대로 정리하였다. 이 결과들은 농장이나 수의사, 컨설턴트들이 옵티팜에 의뢰한 케이스 위주로 분석한 결과이기 때문에 실제 농장에서 발생하는 질병 패턴과는 약간 다른 결과일 수 있음을 고려해 주시기 바란다.
2016년에는 2015년에 비해서 몇 가지 특이점이 발견된다. 먼저 대장균 분리 검사와 호흡기 질병, 그리고 유사산의 전반적인 증가가 눈에 띈다. 최근 양돈현장에서 부종병의 증가가 두드러지고 있어 대장균, 특히 부종병 원인균에 대한 주의가 필요하다. 그리고 추가적으로 2015년에는 볼 수 없었던 몇 가지 질병이 검색되고 있는데 마이코플라즈마 하이오리니스 (Mycoplasma hyorhinis) 돼지싸이토메갈로바이러스감염증 등도 최근 들어 검색이 되고 있다. 좀더 자세히 내용을 살펴보자.
B. 혈청검사
2015년의 경우 총 2,365농가에서 혈청검사 샘플이 접수되었으나 2016년의 경우에는 총 2,711개의 농가에서 혈청검사 샘플이 접수되어 14.6%의 농가수의 증가가 있었다. 혈청검사 의뢰 건수의 경우에는 더 높은 증가율을 보여 2015년에 41,036개의 혈청이 접수된 반면, 2016년에는 48,677개가 접수되어 18.6%의 증가를 보였다. 혈청검사 의뢰 농장과 의뢰 혈청 개수가 증가한 이유는 혈청검사를 통한 농장 질병 모니터링이 중요한 도구로 인식되고 있기 때문인 것으로 판단된다. 특히 종돈장의 경우 PRRS 등 주요 질병에 대한 모니터링을 정기적으로 시행하는 종돈장이 계속 증가하고 있는 것으로 보인다. 또한 구제역에 대한 백신 SP ELISA 검사를 민간병성감정기관에서 검사가 가능해 짐에 따라 이에 따른 증가도 혈청검사 증가의 중요한 원인 중 하나로 파악된다. PRRS항원 검사에서는 전년도 대비 약 30% 가까운 항원 양성 증가가 기록되고 있어 이에 대한 주의가 필요하다. 필자는 개인적으로 PRRS가 우리나라 양돈산업에 있어 매우 중요한 질병이라고 생각한다. 눈에 보이는 폐사 이외에도 사료효율 감소 등 눈에 보이지 않는 피해로 우리나라에서 한 해에만 약 1000억원 가까운 경제적 손실이 발생되고 있는 것으로 추정되고 있다. 그러므로 종돈장과 AI 센터 특성상 정기적인 항원/항체 검사를 하는 것이 필요하며 양돈장에서도 후보돈을 구입하거나 정액을 구입할 때 정기적인 PRRS 검사 성적서를 요구하는 것이 필요하다
C. 돼지생식기호흡기증후군(PRRS : Porcine reproductive and respiratory syndrome)의 특징
2014년 이전에는 우리나라에 북미형 PRRS에 대한 백신 한 종만 판매되었으나 2014년 하반기부터 유럽형 PRRS에 대한 백신이 추가로 판매가 되기 시작했고 2015년 하반기 부터는 Zoetis에서도 북미형 백신을 추가로 판매하고 있어 선택의 폭이 넓어지고 있다. 북미형 바이러스 유래 백신으로는 과거부터 오랜기간 동안 사용해온 베링거인겔하임의 MLV 백신 strain (VR2332 유래)과 Zoetis 백신 (P129 strain)이 있으며 유럽형 바이러스 유래 백신으로는 Hipra의 백신 (VP046 strain)와 MSD 동물약품의 주이다. 북미형 PRRS바이러스와 유럽형 PRRS 바이러스는 유전자가 서로 달라 농장에서 문제되는 PRRS virus에 따라 선택적으로 사용하는 것이 바람직할 것으로 판단된다. 특히 아직도 현장에서는 유럽형 바이러스가 북미형에 대해서, 또 북미형 바이러스가 유럽형에 대해서 교차 반응이 충분한지에 대해서 많이들 궁금해 하는데 필자의 생각에는 북미형 바이러스가 문제되는 농장에는 북미형을, 유럽형이 문제되는 농장에서는 유럽형 백신을 접종하는 것이 가장 바람직할 것으로 생각한다. 이를 확인하기 위해 교차 방어에 대한 연구 논문을 계속 검색하고 있지만 교차 방어에 대한 자료가 많지 않고 해당 농장에 문제되는 바이러스에 대한 정확한 평가를 통해 백신을 선택하는 것이 가장 바람직할 것으로 판단된다.
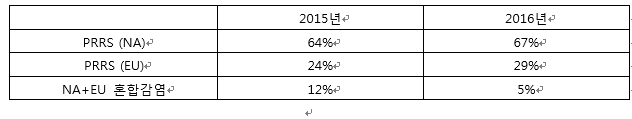
■표 2. 2015년과 2016년 북미형 PRRS 바이러스와 유럽형 PRRS 바이러스, 그리고 혼합 감염의 비율. 최근에는 북미형과 유럽형이 각각 3%, 5% 증가한 반면, 혼합감염 케이스는 7% 감소하였다
(자료출처 : ㈜ 옵티팜).
D. 돼지써코바이러스 (Porcine Circovirus type2 )
옵티팜에서는 지난 1년 동안 195건의 PCV2 항원 검출케이스가 있었다. 2015년에는 168건의 항원 검출케이스가 있어 작년 동기와 비교를 해보았을 때 약 16% 정도 증가했음을 알 수 있다. PCV2 백신을 접종하더라도 조직중에서 항원은 검출될 수 있기 때문에 항원 검출에 큰 의미를 둘 수는 없다. 다만 최근 미국과 유럽 등 양돈 선진국에서 PCV2 백신을 안하는 경향이 있다고 하였는데 필자의 경우에는 최근까지도 국내에서 PCV2 발병 감소로 PCV2 백신을 뺐다가 2008년에 이미 겪었던 것처럼 폐사율이 무려 40% 상황으로 돌아간 예를 직접 보아오고 있다.
미국의 경우 1년에 약 58백만 ~ 60백만 두 분의 PCV2 백신이 사용되어 접종률로는 대략 96~97% 수준이 되는 것으로 추정된다. 백신판매량을 전체 생산 두수로 나누면 나오는 계산인데 실제로는 2회 접종 농장도 포함되어 있기 때문에 아주 정확한 계산을 하기는 거의 불가능하다. 실제 미국 양돈장들에 직접 문의를 하여 PCV2 접종에 대한 조사를 해보니 전체 농가의 약 95%가 PCV2 백신을 접종하고 있다는 답이 돌아왔다.
E. 클로스트리디움 A 타입 감염증 (Clostridium perfringenes Type A)
과거에는 Clostridium perfringenes Type C(CPC)는 중요한 병원체로 다루어졌으나 Clostridium perfringenes Type A (CPA)는 상대적으로 병원성이 약한 세균으로 간주되었다. CPC가 양돈에서 중요한 병원체로 간주되었던 것은 바로 독소의 존재 유무 때문이었다. CPA와 CPC를 보면 CPC의 경우 CPA에 들어있지 않은 독소가 들어 있음을 알 수 있다.
■표 3. CPA와 CPC의 독소 구성의 차이와 임상증상 구분. CPC에는 CPA에 들어있지 않은 beta독소가 들어 있기 때문에 CPA보다 더 강한 출혈 소견과 괴사가 발생할 수 있다.

클로스트리디움 독소중 beta toxin에 대해서는 일본인 학자인 Sakurai라는 분이 많은 연구를 했는데 CPC에 들어 있는 beta 독소의 경우 소장에서 출혈성 점막 궤양 또는 점막면의 괴사를 동반하는 괴사성 장염을 일으키는 것을 그 특징으로 하고 있다 (Sakurai and Fujii 1987).
1998년에 Steinthorsdottir 등은 실로 놀라운 연구결과를 발표했는데 beta toxin에 대해서 총 11군데 변형을 주어 단백질을 만들어 보니 총 336개 아미노산중 212번째에 있는 아르기닌(arginine)이라는 아미노산이 beta toxin의 독성에 매우 중요해서 이 아미노산을 glutamic acid로 치환하자 독성이 무려 11.5배 감소하는 것을 관찰했다. (Steinthorsdottir, Fridriksdottir et al. 1998). 독소에서 단 한 개의 아미노산이 얼마나 중요한 역할을 할 수 있는지 알 수 있는 대목이다. 이 멘트를 쓴 이유는, CPA가 분리되면 모두 같은 CPA라고 생각하기 쉬운데 CPA도 유전자의 차이에 따라 병원성이 크게 달라질 수 있으므로 같은 CPA가 분리되었는데 왜 어떤 때는 어린 자돈에서 괴사성 장염처럼 나타나고, 또 왜 어떤 때는 PED와 구분하기 힘든 수양성 설사를 나타내기도 하는지를 이해하는 게 필요하기 때문이다.
CP beta toxin이 병원성을 나타내는 이유는 세포막에 물질이 드나들 수 있는 채널을 형성해서 세포막에 구멍을 내는 것과 같은 효과를 나타내는데 이렇게 구멍이 난 세포는 세포를 경계로 투과성이 변하여 세포가 결국 망가지게 하는 것이다 (Smedley Iii, Fisher et al. 2004).
그럼 이 beta toxin은 그 자체로 독성을 나타낼 수 있을까? Beta toxin이 포함된 CPC는 장괴사를 일으키지만 beta toxin을 정제하여 동물에 먹여보면 장에 병변을 일으키지 못한다. 한편, 사람의 경우 beta toxin에 대한 toxoid를 만들어 주사를 하는 경우 CPC에 대한 괴사성 장염을 예방할 수 있다. 즉, beta toxin 자체는 괴사성 장염을 일으키는데 결정적인 요소인 것은 맞지만 그 자체로는 병변을 일으킬 수 없고 다른 독소가 있어야 병변을 일으킬 수 있다 (Smedley Iii, Fisher et al. 2004). 불행히도 이 부분, 어떤 요소가 있어야 beta toxin이 비로소 독성을 나타내는지에 대한 연구가 아직 명확하지 않다.
양돈 수의사들이 바이블처럼 보는 Disease of Swine이라는 책을 보면 CPA는 정상세균총이라고 되어 있다 (Straw 2006). 그리고 CP는 동물 뿐만 아니라 토양, 심지어는 고춧가루에서도 검출이 되곤 한다 (Matches, Liston et al. 1974, Aguilera, Stagnitta et al. 2005). 게다가 CPA는 양돈에서 심심찮게 검출이 되며 특별한 증상이 없는 경우에서도 분리가 되고 있다. 그렇다면 CPA는 정말 비병원성, 정상세균총일까?
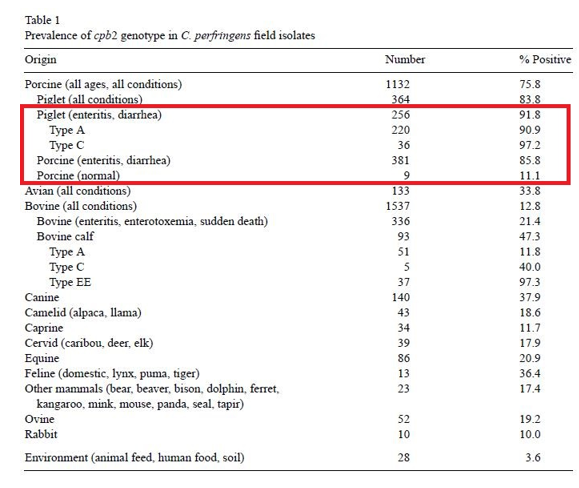
■표 4. CP beta2 toxin에 대한 분석 자료. 어린 자돈의 설사나 장염에서 CP beta2 유전자의 검출비율이 91.8%에 이르며 특히 정상돼지에서는 11.1%, 설사나 장염 개체에서는 85.8%에 이르기 때문에 CP beta2를 CP 진단에서 중요하게 다뤄야 할 것으로 보인다.
F. 유사산의 증가
2016년 병성감정 특징 중 하나는 유사산이 증가했다는 점이다. 원인체로도 돼지싸이토메갈로바이러스 등이 추가되었다. 유사산의 원인으로는 큰 종류로만도 10종이 넘고 개별적인 원인을 각각 분류하면 30종이 넘는다. 유사산의 원인을 정확하게 파악해야 할 이유이다. 그런데 대부분의 농장들이 유사산이 발생하면 정밀 검사없이 넘기곤 한다. 물론 유사산의 원인중에는 영양이나 기후 변화에 의한 것도 있지만 병원체에 의한 유사산일 경우, 정확한 진단이 선행되어야 대책을 마련할 수 있기 때문이다.
G. 항생제 감수성 검사의 필요성
필자가 근무하는 ㈜ 옵티팜 실험실에는 연간 약 800건 정도의 항생제 감수성 검사가 의뢰되고 있다. 주 목적은 항생제를 선택할 때 해당 균이 항생제에 대해서 내성균인지, 감수성 균인지 판별하기 위한 것으로 판단된다. 항생제 감수성/내성에 대한 분석을 해보면 예상보다 항생제 내성이 빨리 생겨 의아하게 생각하는 경우가 많았다.
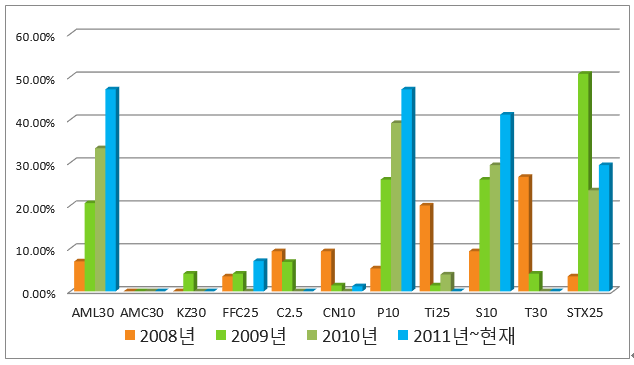
그림 3. 양돈 호흡기 세균들에 대한 항생제 내성 세균 발현 비율에 대한 자료 (자료 출처 : ㈜ 옵티팜). 아목시실린, 페니실린, 스트렙토마이신, Trimethoprim/Sulfamethoxazole 합제의 내성 비율이 계속 증가되는 것을 볼 수 있다.
그림 3를 보면 경구용 산제로 많이 사용되는 아목시실린 (AML30)의 경우 2008년도에 10%도 채 안되던 내성비율이 2011년에는 50% 가까운 내성율을 보이고 있다. 세균이 어떻게 이렇게 빠른 속도로 내성을 획득하는지에 대해서 항상 의문을 가지고 있었는데 최근 하버드 대학교에서 만든 시뮬레이션 자료에서 세균이 높은 농도의 항생제에 대해서 얼마나 빨리 내성을 가질 수 있는지 보여주었다. 일반농장에서는 항생제 감수성/내성 검사 없이 항생제를 쓰는 경우가 있는데 항생제 내성문제를 피하려면 1차 처방 이후 반드시 항생제 감수성/내성 검사를 해서 그 결과를 처방에 반영하는 것이 좋다.

그림 4. 세균이 고농도의 항생제에 대해서 얼마나 빨리 내성을 획득하는지 보여주는 자료. 14리터의 한천 겔에 농도별 항생제를 섞은 다음 대장균을 접종하면 세균이 자라게 된다. 세균이 자라면서 내성을 획득한 돌연변이 (mutant)가 생기게 되고 이 세균은 10일만에 고농도 항생제에 대해서 완벽한 내성을 획득하게 된다.
3. 참고문헌
Aguilera, M. O., P. V. Stagnitta, B. Micalizzi and A. M. S. de Guzmán (2005). "Prevalence and characterization of Clostridium perfringens from spices in Argentina." Anaerobe 11(6): 327-334.
Matches, J. R., J. Liston and D. Curran (1974). "Clostridium perfringens in the environment." Applied microbiology 28(4): 655-660.
Sakurai, J. and Y. Fujii (1987). "Purification and characterization of Clostridium perfringens beta toxin." Toxicon 25(12): 1301-1310.
Smedley Iii, J., D. Fisher, S. Sayeed, G. Chakrabarti and B. McClane (2004). The enteric toxins of Clostridium perfringens. Reviews of physiology, biochemistry and pharmacology, Springer: 183-204.
Steinthorsdottir, V., V. Fridriksdottir, E. Gunnarsson and Ó. S. Andrésson (1998). "Site-directed mutagenesis of Clostridium perfringens beta-toxin: expression of wild-type and mutant toxins in Bacillus subtilis." FEMS microbiology letters 158(1): 17-23.
Straw, B. E. (2006). Diseases of swine. Ames, Iowa, Blackwell Pub.