
"무안군 3km 방역대 구제역 이동제한 해제검사 과정에서 돼지농장 2곳의 축사 바닥 환경 시료에서 바이러스가 검출돼, 해당 농장 돼지 타액 등의 정밀검사를 의뢰한 결과 11일 최종 양성 판정 - 전남도" 종식 선언을 코 앞에 두고 구제역이 추가로 발생했습니다. 그것도 돼지농장에서 말입니다(관련 기사). 국내 돼지농장에서 구제역이 발생한 것은 지난 '18년 경기 김포 사례 이후 7년 만입니다. 당시 백신에 포함되지 않은 A형 바이러스가 원인이었습니다. O형 바이러스에 의한 돼지 구제역은 '16년 전북 김제·고창, 충남 공주·천안·논산·홍성 사례 이후 9년 만입니다. 여하튼 11일 주요 언론은 앞다투어 '7년 만에 돼지 구제역 발생'이라는 제목으로 소식을 전했습니다. 13일에는 '전파력 1000배인 돼지에서 발생'이라는 제목의 기사도 등장했습니다. 소와 비교해 돼지의 경우 구제역에 감염 시 고농도의 바이러스를 배출하는 것으로 알려졌습니다. 한돈산업은 물론이고 특히, 방역당국이 크게 당혹해 하는 분위기입니다. 돼지에서 발생한 자체도 문제지만, 무증상 돌파감염으로 강하게 추정되기 때문입니다. 11일 첫 공식 발표에서 방역당국은 '구제역 긴급 백신접종, 무증상인 점

'돼지 유행성설사 바이러스(PEDV)'는 지난 30년 동안 한국의 양돈산업에 심각한 재정적 위협이 되어 왔습니다. PEDV 감염은 대부분 영향을 받은 '분만-비육(FTF) 돈군'에서 지속되면서, 연중 반복적으로 발생하는 '풍토성 돼지 유행성설사(endemic PED)'으로 이어집니다. 이 보고서는 한국의 풍토성 PEDV 지속성에 대한 현재 상황과 통제 조치에 대한 개요를 제공합니다. 2013-2014년 PED 대유행 이후, HP-G2b PEDV는 국내에서 우세한 균주가 되었으며 계속 진화하여 소규모의 유전적 다양성을 형성하고 있습니다. 국내 HP-G2b 균주는 최근(2022년 초)까지 육지부 3개 클레이드와 제주도 2개 클레이드를 포함한 6개 지역 특이 클레이드로 유전적으로 구분되었으나, 현재는 육지와 제주도에서 거의 동시에 출현한 2개의 서브클레이드인 CK.1과 CK.2를 포함한 8개 클레이드로 분류되고 있습니다. 최근까지 HP-G2b PEDV에 효과적인 경구용 백신이 없어 '4가지 핵심 방역 전략(차단방역, 백신접종, 신속한 진단·능동적인 모니터링/감시, 돈군관리)'에서 빠진 조각이었지만, 경구용 G2b 백신의 국내 출시로 이를 완성할 수 있게 됐습니다.
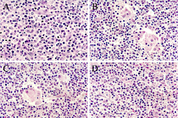
이번 연구의 목적은 '돼지 써코바이러스 2형(PCV2d)'의 병원성을 확인하는 것이었습니다. 비강 내 PCV2d 단독, PCV2d와 마이코플라즈마 하이오뉴모니아에(M. hyopneumoniae, 유행성폐렴균), PCV2d와 돼지생식기호흡기증후군바이러스(PRRSV)를 각각 접종하는 방식으로 진행되었습니다. 실험 결과 PCV2d 단독으로 감염시킨 돼지는 무증상이었습니다. 유행성폐렴균과 PCV2d 또는 PCV2d와 PRRSV를 접종한 모든 돼지는 갑작스러운 임상 증상과 파종성 육아종성 염증을 특징으로 하는 돼지 써코바이러스 연관 질병(PCVAD)이 발생했습니다. 염증은 주로 림프절과 비장에 나타났으며 간혹 간과 신장에 나타나기도 했습니다. 이들 두 그룹의 돼지는 PCV2d만 접종한 돼지보다 현미경 림프 병변 점수가 유의하게 높았고(P <0.05), 림프절 조직에서 'PCV2 양성 세포(PCV2-positive cells)'의 수가 유의하게 높았습니다(P <0.05). 유행성폐렴균과 PRRSV를 함께 감염시키면 혈중 PCV2d 부하가 강화되었습니다(편집자주; 바이러스혈증). PRRSV와 PCV2d를 병용 감염시켰을 때 유행성폐렴균과 PCV2d를 병용 감염